L’essentiel à retenir
—
⏱ ~8 min
L’acide iodique est un composé inorganique essentiel, pourtant potentiellement dangereux. Son utilisation requiert des connaissances spécifiques.
- 🎯 Comprendre ses propriétés est crucial.
- ⚡ Utiliser des protections lors de la manipulation.
- ⏰ Informer sur ses effets en cas d’exposition.
- ⚠️ Ne pas oublier d’évaluer ses interactions avec d’autres substances.
Acide iodique (HIO3) : Structure et Propriétés
L’acide iodique, ou HIO3, est un acide oxo qui possède des caractéristiques chimiques notables. Sa structure est basée sur un atome d’iode entouré de trois atomes d’oxygène, ce qui lui confère un état d’oxydation de +5. Ce composé inorganique est bien plus qu’un simple acide ; il est utilisé dans divers domaines, allant de la chimie analytique à la stérilisation.
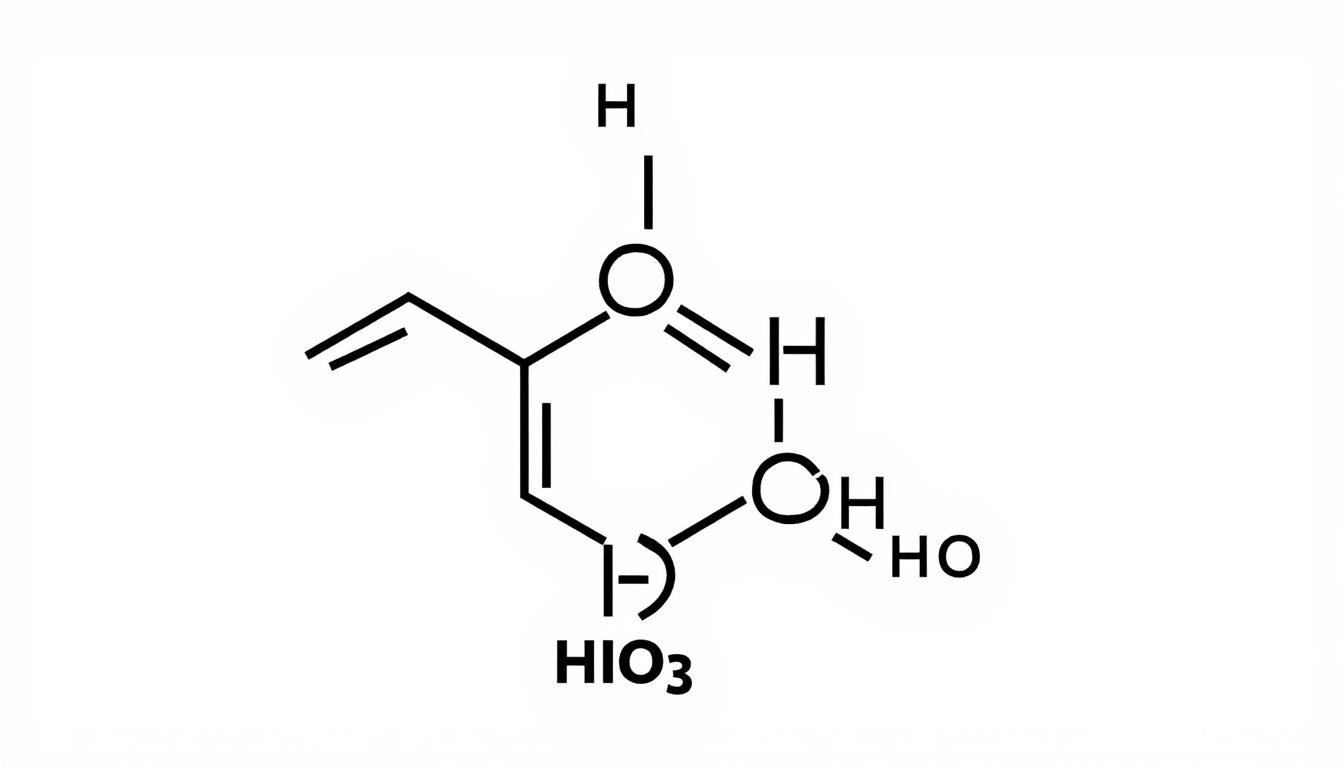
Voici quelques-unes de ses propriétés :
- État physique : solide cristallin, blanc.
- Masse moléculaire : 175,91 g/mol.
- Densité : 4,629 g/ml à 20 °C.
- Solubilité : 2 690 g/l dans l’eau à 20 °C.
Cette haute solubilité en fait un agent efficace dans plusieurs applications. En raison de sa nature oxydante, il peut participer à de nombreuses réactions chimiques. Il est essentiel de connaître ces propriétés pour une manipulation sécurisée.
Caractéristiques physiques et chimiques
La manipulation de cet acide nécessite une compréhension claire de ses propriétés physiques et chimiques. Par exemple, l’acide iodique est réputé pour sa capacité à décomposer certains éléments sous chaleur, ce qui peut générer des gaz toxiques.
Les réactifs qui peuvent entrer en conflit avec HIO3 comprennent :
- Les agents réducteurs.
- Les acides forts comme l’acide sulfurique.
- Les composés organiques, qui peuvent s’enflammer en présence d’acide iodique.
Lors de son stockage, il est crucial de le garder à l’abri de la chaleur et des matières combustibles. En cas de déversement, seul un personnel formé et équipé devrait intervenir, en respectant les protocoles de sécurité recommandés.
Dangers associés à l’acide iodique
Bien que l’acide iodique soit utilisé dans divers secteurs, il présente aussi des dangers potentiels. Son exposition peut avoir des conséquences graves, notamment des irritations cutanées et des dommages aux voies respiratoires.

Différents types de risques sont à considérer :
- Contact cutané : corrosif, peut provoquer des brûlures.
- Contact oculaire : irritant, peut entraîner des lésions permanentes.
- Inhalation de vapeurs : irritations sévères des voies respiratoires.
- Ingestion : entraîne des douleurs abdominales et des symptômes gastro-intestinaux.
Il est donc essentiel d’utiliser des équipements de protection individuelle (EPI) adéquats lors de la manipulation de cet acide. Parmi ces équipements, on retrouve :
- Des gants en caoutchouc, pour protéger la peau.
- Des lunettes de protection, pour éviter les éclaboussures.
- Des masques respirateurs, en cas d’inhalation de poussières ou de vapeurs.
Un manque de sensibilisation aux dangers peut conduire à des accidents graves. Pour réduire ces risques, des formations régulières sur la sécurité chimique devraient être intégrées dans les protocoles de travail.
Utilisations de l’acide iodique
L’acide iodique est largement utilisé dans plusieurs domaines. Sa polyvalence en fait un composé crucial dans certaines industries. Voici quelques exemples d’applications :
- Chimie analytique : Utilisé pour les titrages et les analyses quantitatives d’autres substances chimiques.
- Laboratoires de recherche : Souvent employé pour orienter des expériences sur l’iode et ses dérivés.
- Désinfection : L’acide iodique est parfois intégré dans des solutions pour stériliser divers surfaces.
- Industrie pharmaceutique : Joue un rôle clé dans la fabrication de certains médicaments contenant de l’iode.
Des études montrent que les propriétés oxydantes de HIO3 permettent de l’utiliser comme agent de purification pour plusieurs composés. Toutefois, ces applications doivent être manipulées avec précaution, compte tenu de sa toxicité.
Tableau des principales applications de l’acide iodique
| Application | Description |
|---|---|
| Chimie analytique | Utilisé pour des titrages précis et la détermination de concentrations. |
| Désinfection | Agent purifiant pour équipements médicaux et surfaces. |
| Recherche | Essentiel pour des études sur les composés iodés. |
| Industrie pharmaceutique | Ingrédient dans la fabrication de médicaments spécifiques. |
Risques d’exposition à l’acide iodique
Un usage inapproprié de l’acide iodique peut avoir des impacts significatifs sur la santé. Malheureusement, de nombreux utilisateurs ne prennent pas suffisamment au sérieux ces dangers. Voici ce qu’il faut savoir sur les risques d’exposition :
- Les effets aigus incluent des brûlures, en particulier pour la peau et les yeux.
- Des symptômes respiratoires peuvent apparaître rapidement, comme une toux persistante.
- Les effets chroniques peuvent comprendre des troubles endocriniens dus à une exposition répétée.
La réponse du corps à cet acide peut varier selon les individus. Certaines personnes, particulièrement celles souffrant de maladies auto-immunes, peuvent réagir plus fortement. Une surveillance médicale régulière est recommandée, surtout pour ceux qui manipulent cet acide régulièrement.
Il est crucial d’informer le personnel sur les moyens de gestion des accidents, tels que :
- Éviter le contact avec la peau et rincer abondamment à l’eau.
- Consulter un médecin en cas d’inhalation ou ingestion.
- Suivre des protocoles d’évacuation en cas de déversement.
Évaluation et réglementation de l’acide iodique
Face à des risques potentiels, les régulations entourant l’acide iodique sont strictes. Les agences nationales de sécurité évaluent régulièrement les dangers associés aux produits chimiques. En France, l’ANSES (Agence nationale de sécurité sanitaire de l’alimentation, de l’environnement et du travail) fixe des directives claires pour sa manipulation.
Il est indispensable de respecter les limites d’exposition établies par la réglementation. En général, les travailleurs ne doivent pas dépasser 600 µg/jour d’exposition à l’iodine. Cela permet de minimiser le risque de toxicité. Les mesures de prévention doivent être vérifiées régulièrement.
Gestion des déchets d’acide iodique
Se débarrasser des déchets d’acide iodique de manière responsable est crucial pour la sécurité environnementale. Les déchets doivent être manipulés avec prudence. Il est déconseillé de les déverser dans les égouts ou dans la nature. Les déchets solides doivent être placés dans des contenants hermétiques et étiquetés correctement.
Un approvisionnement adéquat en équipements de traitement des déchets doit être en place pour garantir un traitement approprié. Les étapes recommandées sont :
- Collecte des déchets dans des contenants spécifiés.
- Transport vers une installation de traitement des déchets en accord avec la réglementation.
- Documentation de l’élimination pour les audits de conformité.
Les projets de nettoyage doivent être planifiés en tenant compte des risques d’exposition pour les personnes impliquées.
Questions fréquentes
Voici quelques questions courantes concernant l’acide iodique :
Quels sont les effets d’une exposition à l’acide iodique ?
Une exposition peut causer des irritations sévères de la peau et des voies respiratoires.
Il est crucial de porter des protections adéquates pour éviter ces risques.
Comment stocker l’acide iodique en sécurité ?
Il doit être conservé dans un endroit frais, sombre, et aéré, à l’abri des matières combustibles.
Utilisez des contenants hermétiques pour limiter les risques.
Quelle est sa masse molaire ?
La masse molaire de l’acide iodique est de 175,91 g/mol.
Cette information est cruciale pour les calculs en chimie analytique.
Quels secteurs utilisent l’acide iodique ?
Il est principalement utilisé dans la chimie analytique, la recherche et l’industrie pharmaceutique.
Sa polyvalence en fait un outil précieux dans de nombreux laboratoires.