Introduction
Les éléments chimiques se divisent en trois catégories fondamentales ⁚ les métaux, les non-métaux et les métalloïdes, qui présentent des propriétés physiques et chimiques distinctes.
Définitions et classification des éléments chimiques
La classification des éléments chimiques en métaux, non-métaux et métalloïdes repose sur leurs propriétés physiques et chimiques. Les métaux sont des éléments qui présentent une haute conductivité électrique, une ductilité et une malléabilité élevées, ainsi qu’une tendance à perdre des électrons pour former des ions positifs. Les non-métaux, au contraire, ont une faible conductivité électrique et une tendance à gagner des électrons pour former des ions négatifs. Les métalloïdes, également appelés semi-métaux, occupent une position intermédiaire entre les métaux et les non-métaux, avec des propriétés partagées entre ces deux groupes.
Cette classification permet de regrouper les éléments chimiques en familles, telles que les métaux alcalins, les métaux alcalino-terreux, les métaux de transition, les non-métaux nobles, les gaz nobles et les demi-métaux, qui sont disposés de manière spécifique dans le tableau périodique.
Les Métaux
Les métaux sont des éléments chimiques caractérisés par une haute conductivité électrique, une ductilité et une malléabilité élevées, ainsi qu’une tendance à perdre des électrons.
Les métaux possèdent des propriétés physiques telles que la ductilité, la malléabilité et la conductivité électrique. Ils ont également des propriétés chimiques caractéristiques, comme la réactivité et la tendance à perdre des électrons pour former des ions positifs. Ces propriétés varient en fonction de la position de l’élément dans le tableau périodique. Les métaux sont généralement solides à température ambiante, sauf quelques exceptions comme le mercure qui est liquide. Ils peuvent également avoir des points de fusion et d’ébullition élevés. Les propriétés physiques et chimiques des métaux déterminent leurs utilisations et applications dans divers domaines tels que la construction, l’électronique et l’industrie.
Exemples de métaux ⁚ métaux alcalins, métaux alcalino-terreux et métaux de transition
Les métaux alcalins, tels que le sodium, le potassium et le lithium, sont très réactifs et ont une faible densité. Les métaux alcalino-terreux, comme le magnésium, le calcium et le strontium, sont moins réactifs que les métaux alcalins mais plus que les métaux de transition. Les métaux de transition, tels que le fer, le cuivre et le zinc, sont caractérisés par leur capacité à former des ions de différents états d’oxydation. Ces métaux ont des propriétés magnétiques et des applications variées, notamment dans la fabrication d’alliages et de catalyseurs. Les exemples de ces métaux montrent la diversité des propriétés physiques et chimiques au sein de la famille des métaux.
Les Non-Métaux
Les non-métaux sont des éléments chimiques qui ne possèdent pas les propriétés caractéristiques des métaux, telles que la conductivité électrique et la ductilité.
Les non-métaux présentent des propriétés physiques et chimiques spécifiques, telles que une faible conductivité électrique, une résistance élevée à la corrosion et une forte réactivité.
Ils peuvent être solides, liquides ou gazeux à température ambiante et ont généralement une densité plus faible que les métaux.
Dans le tableau périodique, les non-métaux occupent la majorité des cases situées à droite de la diagonale qui sépare les métaux des non-métaux.
Ces éléments chimiques ont tendance à gagner ou à partager des électrons pour former des liaisons covalentes, ce qui leur confère des propriétés différentes de celles des métaux.
Exemples de non-métaux ⁚ non-métaux nobles, gaz nobles et demi-métaux
Les non-métaux nobles, tels que l’hélium (He), le néon (Ne) et l’argon (Ar), sont des gaz rares qui ne réagissent pas avec d’autres éléments.
Les gaz nobles, comme le krypton (Kr) et le xénon (Xe), possèdent des configurations électroniques particulières qui les rendent très stables.
Les demi-métaux, tels que le bore (B) et le silicium (Si), présentent des propriétés intermédiaires entre celles des métaux et des non-métaux.
Ces éléments chimiques ont des applications variées dans les domaines de la physique, de la chimie et de la technologie.
Les Métalloïdes
Les métalloïdes, également appelés semi-métaux, sont des éléments chimiques qui partagent des propriétés avec les métaux et les non-métaux.
Propriétés physiques et chimiques
Les métaux présentent des propriétés physiques telles que la conductivité électrique, la ductilité et la malléabilité. Ils ont également des propriétés chimiques comme la réactivité et la tendance à perdre des électrons pour former des ions positifs.
Ils peuvent être divisés en plusieurs groupes, tels que les métaux alcalins, les métaux alcalino-terreux et les métaux de transition, qui ont des propriétés spécifiques.
Ces propriétés physiques et chimiques permettent aux métaux d’avoir des applications variées dans la vie quotidienne, allant des objets de décoration aux équipements électroniques.
Exemples de métalloïdes ⁚ semi-métaux
Les métalloïdes, également appelés semi-métaux, occupent une position intermédiaire entre les métaux et les non-métaux dans le tableau périodique.
Ils partagent certaines propriétés avec les métaux, comme la conductivité électrique, mais possèdent également des propriétés non métalliques, telles que la faible ductilité et la malléabilité.
Des exemples de métalloïdes incluent le silicium, le germanium, l’arsenic, l’antimoine et le tellure, qui sont utilisés dans divers domaines, tels que l’électronique, les semiconducteurs et les matériaux de construction.
Caractéristiques Communes et Différences
Les métaux, non-métaux et métalloïdes présentent des caractéristiques communes et distinctes, telles que la conductivité électrique, la ductilité, la malléabilité, la corrosion et la réactivité.
Conductivité électrique, ductilité, malléabilité, corrosion et réactivité
Les métaux se caractérisent par une grande conductivité électrique, due à la présence d’électrons libres. Ils sont également ductiles et malléables, ce qui signifie qu’ils peuvent être étirés et façonnés sans se briser. Cependant, ils sont sensibles à la corrosion, qui est accélérée par l’exposition à l’air et à l’eau. Les non-métaux, quant à eux, sont généralement isolants électriques et cassants, tandis que les métalloïdes présentent des propriétés intermédiaires. La réactivité est également un critère de distinction entre ces trois catégories d’éléments, les métaux tendant à perdre des électrons pour former des ions positifs, tandis que les non-métaux tendent à gagner des électrons pour former des ions négatifs.
En résumé, les métaux, non-métaux et métalloïdes se distinguent par leurs propriétés physiques et chimiques, occupant des places spécifiques dans le tableau périodique.
Récapitulation des familles d’éléments et leur place dans le tableau périodique
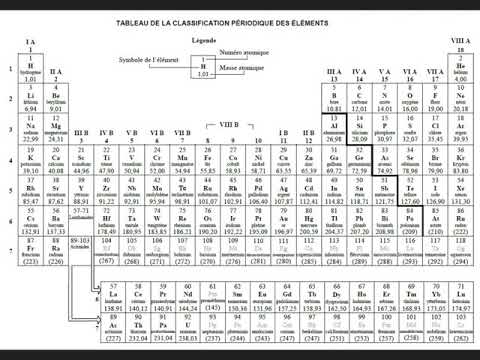
Le tableau périodique permet de classifier les éléments chimiques en fonction de leurs propriétés physiques et chimiques. Les métaux alcalins, alcalino-terreux et de transition occupent la partie gauche du tableau, tandis que les non-métaux nobles, gaz nobles et demi-métaux sont situés à droite. Les métalloïdes, tels que les semi-métaux, se trouvent à la frontière entre les métaux et les non-métaux. Cette disposition permet de mettre en évidence les tendances périodiques et les relations entre les éléments chimiques. La compréhension de ces familles d’éléments et de leur place dans le tableau périodique est essentielle pour étudier les propriétés et les comportements des éléments chimiques.